随着我国医疗事业的发展和部分医院设备的更新换代,我国医疗器械设备的市场需求急剧增长,客观上推动了我国医疗器械设备行业的发展。医疗器械的选用会越来越先进,其产品结构会不断调整,功能更加多样化,市场容量会不断扩大。
对于部分企业其产品的的研究设计初没有多大的考虑到其电磁兼容方面等信息,在医疗设备做备案或者申请医疗注册证时导致不能一次性顺利通过。
医疗器械设备产品分为三大类:
1.诊断设备类;
2.治疗设备类;
3.辅助设备类。
医疗器械测试,医疗注册常用标准:
医疗器械EMC YY0505 GB/T18268.26 IEC/EN60601-1-2
医疗器械安规 GB9706.1 IEC/EN 60601-1
相关标准:
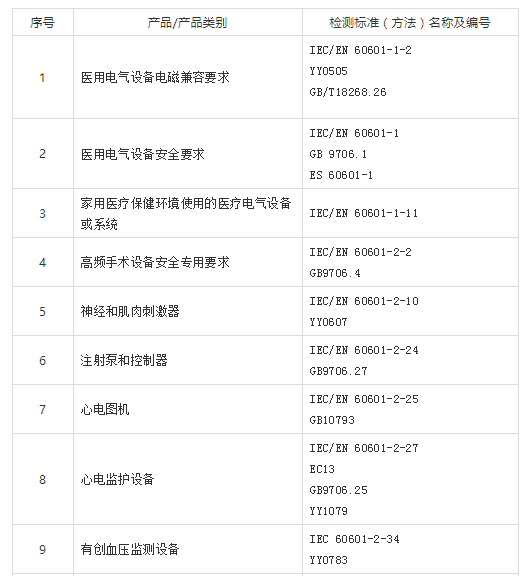
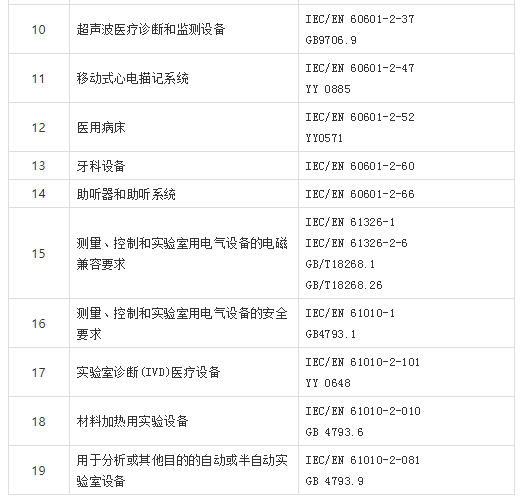
四、医疗器械设备EMC测试项目
空间辐射Radiated
传导骚扰Conduction
谐波电流Harmonic
电压闪烁Filcker
静电ESD
电源快速脉冲群EFT
电源浪涌Surge
工频磁场/磁场抗扰M/S
交流电压跌落Voltage DIPS
辐射抗干扰RS
电源传导抗扰度CS
五、医疗器械设备安规测试项目
危险电压测试
防触电测试
标签耐久性测试
插头放电测试
保护接地测试
抗电强度测试
球压测试
工作电压测试
电源线拉力测试
稳定性测试
温升测试
异常工作测试
扭力测试
冲击测试
跌落测试
震动测试
六、华检EMC整改服务流程
1.项目评估,了解产品目前在EMC测试时遇到的问题点,根据项目评估制定报价单。对产品性能、工作原理等熟悉,评估项目的难易度,制定保密协议;
2.签订合同,开案;
3.摸底定位:
定位出产品干扰源,寻找问题点;
定位出产品干扰路径;
进行针对性整改;
制定出整改报告,整改位置,及详细整改内容;
4.最终验证:
对改板后新样机进行测试;
对改板后新样机进行成本控制;
输出最终验证测试报告;
制定出整改报告,整改位置,及详细整改内容;
5.服务优势:
专业的医疗器械检测设备
相对稳定的检测团队
经验丰富的医疗设备检测认证工程师
保持与机构和咨询公司良好的沟通
华检检测拥有全套的EMC电磁兼容、LVD安全检测设备,设备完全符合IEC/EN60601-1-2(电磁兼容)标准,IEC/EN60601-1(安规安全),YY0505-2012,GB/T18268.26(国内医疗器械EMC检测标准)。GB9706.1(国内医疗器械LVD安规标准)的规范要求。可为医疗器械(医用电子设备)提供全套全项的检测服务,华检检测实验室拥有以上标准的CNA 、CNAS 资质,出具的报告全球互认,国家认可,可用于医疗设备CFDA注册或医疗设备备案,更权威更可靠。
想了解更多的检验检测认证相关信息,欢迎关注我们!
Copyright © 2019 深圳市华检检测技术有限公司 华检实验室 版权所有
深圳市南山区沙河西路3011号白沙科技(新兴)产业园1栋1楼A区 粤ICP备11004009号
华检实验室主营业务:EMC测试、EMC检测、CE认证、FCC认证 、PSE认证、TELEC认证、SAA认证、RCM认证、SRRC认证、CCC认证、医疗器械EMC检测、车载EMC检测、电池CB认证、电池IEC62133报告、UL1642报告、UL2054报告。